Константа електролітичної дисоціації
Константа електролітичної дисоціації (Kд) характеризує рівновагу системи електролітичного розчину – це більш загальна кількісна характеристика (порівняно зі ступенем дисоціації) сили електролітів. Чим більше константа дисоціації, тим сильніше дисоціює електроліт, тобто він легше розпадається на іони, яких у розчині стає багато, і електроліт стає сильним.
Раніше вже говорилося, що в розчині слабкого електроліту встановлюється рівновага, коли швидкість дисоціації в розчині дорівнює швидкості асоціації (див. Електролітична дисоціація):

- [K+] – молярна рівноважна концентрація катіонів;
- [A–] – молярна рівноважна концентрація аніонів;
- [KA] – молярна рівноважна концентрація недисоційованої молекули електроліту.
На відміну від ступеня дисоціації константа дисоціації (для слабкого електроліту) залежить від концентрації розчину.
Ступінь дисоціації та константа дисоціації пов’язані співвідношенням (c – молярна концентрація електроліту):
![]()
Для слабких електролітів константа дисоціації мала, тому нею можна знехтувати:
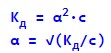
Для сильних електролітів константа дисоціації є змінною величиною, яка залежить від концентрації розчину.

