Що таке хімічний зв’язок
Хімічній зв’язок – це сила, яка утримує разом певну кількість атомів (іонів), забезпечуючи тим самим стабільність утвореної молекули.
Всі речовини в нашому світі складаються з атомів, молекул та іонів, однак, тільки благородні (інертні) гази присутні у вигляді вільних атомів: гелій, неон, аргон, криптон, ксенон, радон. Всі інші хімічні елементи у вигляді вільних атомів у природі не зустрічаються, що пояснюється нестійкістю (незавершеністю) зовнішніх електронних оболонок.
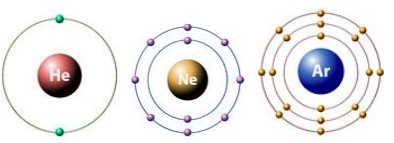
Як видно з малюнків, зовнішні електронні рівні інертних газів повністю укомплектовані, тому вони не віддають та не приймають електрони від інших хімічних елементів (не вступають із ними у хімічні реакції).
Атоми інших хімічних елементів (крім інертних газів) прагнуть завершити свої зовнішні електронні оболонки, віддаючи чи приймаючи електрони від атомів інших хімічних елементів (такі атоми вступають у хімічні реакції).
Водень
Розглянемо найпростіший хімічний елемент – водень, який має лише один електрон. Як тільки два атоми водню зіткнуться один з одним, відразу ж буде утворено молекулу водню Н2 шляхом об’єднання електронів двох атомів. Утворюється електронна пара, що з’єднує між собою обидва атоми водню, які утримуються силою хімічного зв’язку (у молекулі водню кожен атом має завершений рівень із двох електронів).
Сила хімічного зв’язку залежить від електронної будови атомів, які утворюють цей самий зв’язок – чим міцніший хімічний зв’язок, тим стабільнішою є молекула речовини.
Як правило, у встановленні хімічного зв’язку беруть участь електрони, розташовані на зовнішньому (рідше – на попередньому) енергетичному рівні. Такі електрони називаються валентними (див. Валентність).
Число електронів, розташованих на зовнішньому електронному рівні, при яких буде сформовано хімічний зв’язок, для елементів першого періоду періодичної таблиці Д. І. Менделєєва дорівнює 2, для другого та третього = 8, для четвертого та п’ятого = 18 (що відповідає кількості електронів на заповнених оболонках інертних газів).
Електронна теорія валентності говорить, що при утворенні хімічного зв’язку атоми прагнуть сформувати електронну конфігурацію інертного газу.
Таке “завдання” атоми можуть “вирішувати” двома шляхами:
- за рахунок втрати чи придбання електронів від інших атомів (іонний зв’язок);
- з допомогою спільного використання електронів з іншими атомами (ковалентний зв’язок).

