Приклади вирішення задач на молярний об’єм
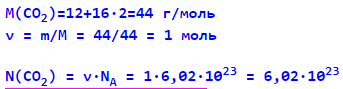
Завдання 1. Скільки молей та молекул міститься у 44 г вуглекислого газу.
Рішення:
Завдання 2. Обчислити масу однієї молекули озону та атома аргону.
Рішення:

Завдання 3. Який обсяг за н.у. займає 2 моля метану.
Рішення:
![]()
Завдання 4. Визначити щільність та відносну щільність оксиду вуглецю (IV) за воднем, метаном та повітрям.
Рішення:

Завдання 5. Визначити масу газової суміші, куди входять 2,8 кубометрів метану і 1,12 кубометрів оксиду вуглецю.
Рішення:

Завдання 6. Визначити об’єми кисню та повітря, необхідні для спалювання 112 кубометрів двовалентного оксиду вуглецю при вмісті в ньому негорючих домішок в об’ємних частках 0,50.
Рішення:
- визначаємо обсяг чистого CO в суміші:
V(CO)=112·0,5=66 кубометрів
- визначаємо об’єм кисню, необхідний для спалювання 66 кубів CO:

або
![]()
- V – молярні об’єми
- V0 – обчислювані об’єми
![]()
Завдання 7. Як зміниться тиск у посудині, заповненій газами водню та хлору після того, як вони вступлять у реакцію? Аналогічно для водню та кисню?
Рішення:
H2+Cl2=2HCl – в результаті взаємодії 1 моля водню і 1 моля хлору виходить 2 моля хлороводню: 1(моль)+1(моль)=2(моль), отже, тиск не зміниться, оскільки об’єм газової суміші, що вийшов, дорівнює сумі обсягів компонентів, що вступили у реакцію.
2H2+O2=2H2O – 2(моль)+1(моль)=2(моль) – тиск у посудині зменшиться у півтора рази, оскільки з 3 обсягів компонентів, що вступили в реакцію, вийшло 2 обсяги газової суміші.
Задача 8. 12 літрів газової суміші з аміаку та чотиривалентного оксиду вуглецю при н.у. мають масу 18 г. Скільки у суміші кожного з газів?
Рішення:

Система рівнянь
- об’єм суміші: x+y=12
маса суміші:
- x/(22,4·17)+y/(22,4·44)=18
Після рішення отримаємо:
- x=4,62 л
- y=7,38 л
Завдання 9. Яка кількість води вийде в результаті реакції 2 г водню і 24 г кисню.
Рішення:
![]()
З рівняння реакції видно, що кількість реагуючих речовин не відповідають відношенню стехіометричних коефіцієнтів у рівнянні. У таких випадках обчислення проводять за речовиною, якої менше, тобто ця речовина закінчиться першою в ході реакції. Щоб визначити якого із компонентів не вистачає, треба звернути увагу на коефіцієнті в рівнянні реакції.
Кількість вихідних компонентів
![]()
Однак поспішати не треба. У нашому випадку для реакції з 1,5 моль кисню необхідно 3 моль водню (1,5·2), а в нас його лише 2 моль, тобто не вистачає 1 моль водню, щоб прореагували всі півтора моля кисню. Тому, розрахунок кількості води будемо вести по водню:
![]()
Завдання 10. При температурі 400 К та тиску 3 атмосфери газ займає об’єм 1 літр. Який обсяг займатиме цей газ за н.у.?
Рішення:
З рівняння Клапейрона:


